Школа по плазмохимии для молодых ученых России и стран СНГ
[ О Школе|Лекции|Секция 1|Секция 2|Секция 3|Секция 4|Секция 5|Cодержание |
ИССЛЕДОВАНИЕ РАСПРЕДЕЛЕНИЯ АТОМОВ CS В ПОГРАНИЧНОМ СЛОЕ ПОТОКА ПРОДУКТОВ СГОРАНИЯ НА ПЛОСКОЙ НЕОХЛАЖДАЕМОЙ ПЛАСТИНЕ
Рогов Б.В., Хомкин М.А.
vladimir@hedric.msk.su, wisnu@oivtran.iitp.ru
Научно-исследовательский центр теплофизики импульсных воздействий РАН, Москва
Введение. Исследование пристеночной плазмы и особенностей распределения плазменных компонент в пограничном слое при обтекании потоком продуктов сгорания металлической поверхности позволяет получить информацию о константах скоростей протекающих в плазме реакций. Интерес к этому вопросу продиктован как с прикладной (проектирование плазменных и энергетических устройств) так и с научной (исследование процессов горения, потенциалов межчастичного взаимодействия) точек зрения.
В настоящей работе приводятся результаты эксперимента по измерению профилей температуры и концентраций атомов присадки цезия в пограничном слое продуктов сгорания пропан-воздушного пламени при обтекании плоской неохлаждаемой пластины. Измеренные профили температуры и концентраций сравнивались с результатами расчетов в рамках модели химически неравновесного ламинарного пограничного слоя [1,2]. Из этого сравнения уточнены константы скоростей ряда химических реакций.
Методика измерений. Поток плазмы продуктов сгорания создавался двухфакельной горелкой типа Меккера. Пограничный слой формировался на поверхности неохлаждаемой (Tw» 1100K) продольно обтекаемой пластины. Температура плазмы измерялась обобщенным методом обращения. Концентрация свободных атомов цезия определялась методом полного поглощения [3]. При этом были использованы кривые роста, рассчитанные с учетом сверхтонкого расщепления атомных уровней цезия.
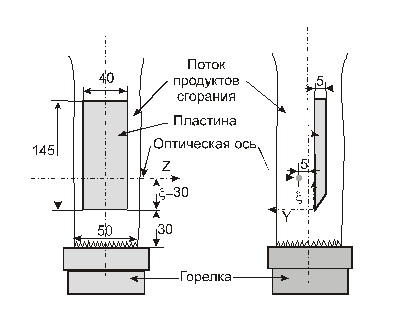
Проведены измерения в сечении пограничного слоя, находящегося на расстоянии x =30мм от передней кромки пластины. В свою очередь передняя кромка пластины находилась на расстоянии 30мм над срезом горелки Меккера (см. Рис.1). В процессе эксперимента варьировался коэффициент избытка окислителя a от 0.9 до 1.20. Режим по a выставлялся по ротаметрам с погрешностью 3%.
Модель неравновесного пограничного слоя. В расчетах использовалась модель химической кинетики, которая учитывает протекание в плазме следующих реакций с участием Cs, CsOH, CsO2, CsO:
| Cs+O2+M=CsO2+M Cs+OH+M=CsOH+M CsOH+H=Cs+H2O NsO2+OH=CsOH+O2 CsO2+H=CsO+OH CsO+H2O=CsOH+OH |
(1) (2) (3) (4) (5) (6) |
Кроме того, при численном моделировании анализировалось влияние на вышеуказанные Cs-содержащие компоненты наличия в газовой смеси газофазного гидрата цезия CsH, химическая кинетика которого моделировалась аналогично кинетике для KH [4].
Константы скоростей этих реакций Kf [см, молекула, с] приведены в Табл.1, там же указаны работы, из которых эти константы взяты. Константы скоростей обратных реакций вычислялись как отношение констант скоростей прямых реакций и констант равновесия. Для оценки констант скоростей бимолекулярных реакций, экспериментальные данные по которым отсутствуют, использовалась теория столкновений [5] и предположение о близости вероятностей однотипных реакций с участием атомов различных щелочных металлов. При расчете констант равновесия, коэффициенты в показателях экспонент вычислялись по значениям энтальпий образования компонент при Т=0, предэкспоненты вычислены по приведенным энергиям Гиббса компонент и аппроксимированы степенными функциями. Необходимые для расчета энтальпий образования СsO2, CsOH, CsO энергии диссоциации были получены на основе обзора литературных данных: D(Сs-O2) = (2,00± 0,17) eV, D(Cs-OH) = (3,89± 0,12) eV, D(Cs-O) = (2,89± 0,29) eV. Энтальпии образования для остальных компонентов были взяты из [6]. Коэффициенты диффузии для отдельных компонент вычислялись по методике [5] в предположении межмолекулярного потенциала Леннарда-Джонса, параметры которого либо брались из литературы [7], либо оценивались по правилам комбинирования [5].
Табл.1.
| ? | Реакции | Константа реакции | T, K | Источник |
| F1 | Cs+O2+M | |||
| M=N2 | [8] | |||
| M=Ar | 325 | [9] | ||
| F2 | Cs+OH+M | |||
| M=He | [10] | |||
| F3 | CsOH+H | Оценка данной работы | ||
| F4 | CsO2+OH | Оценка данной работы | ||
| R5 | CsO+OH | Оценка данной работы | ||
| F6 | CsO+H2O | Оценка данной работы |
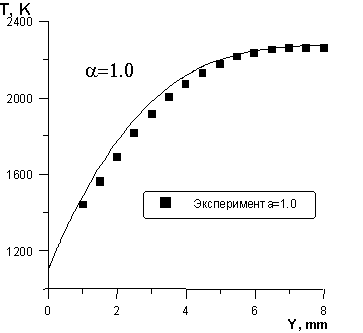
Результаты измерений и расчетов. На Рис.2 изображены расчетные и экспериментальные профили температуры поперек пограничного слоя для a =1.00, x =30мм. Погрешность измерения температуры составляла » 2%.
 |
 |
||
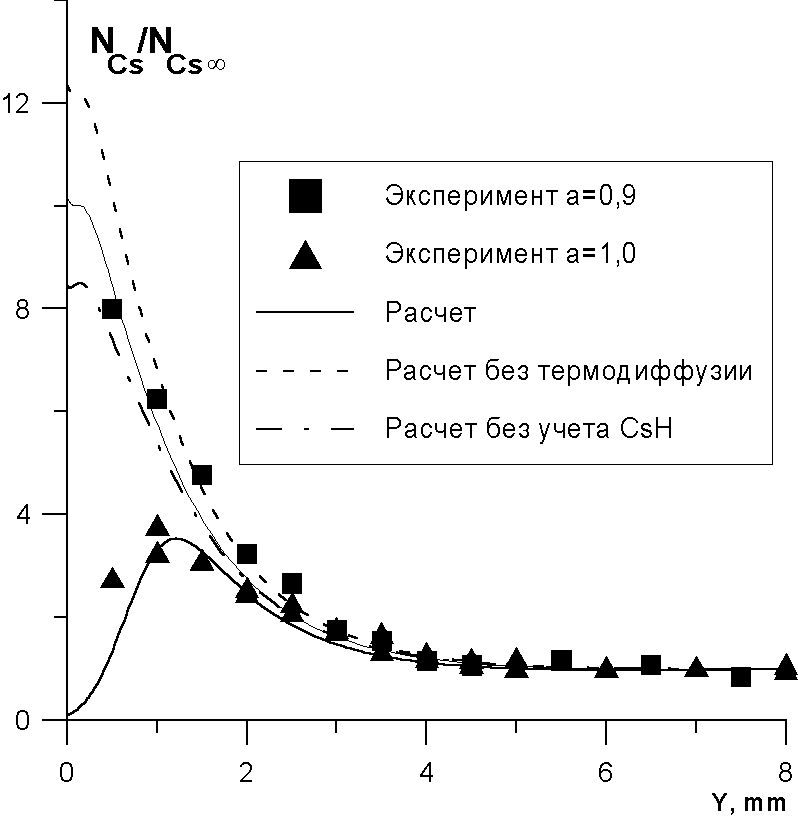
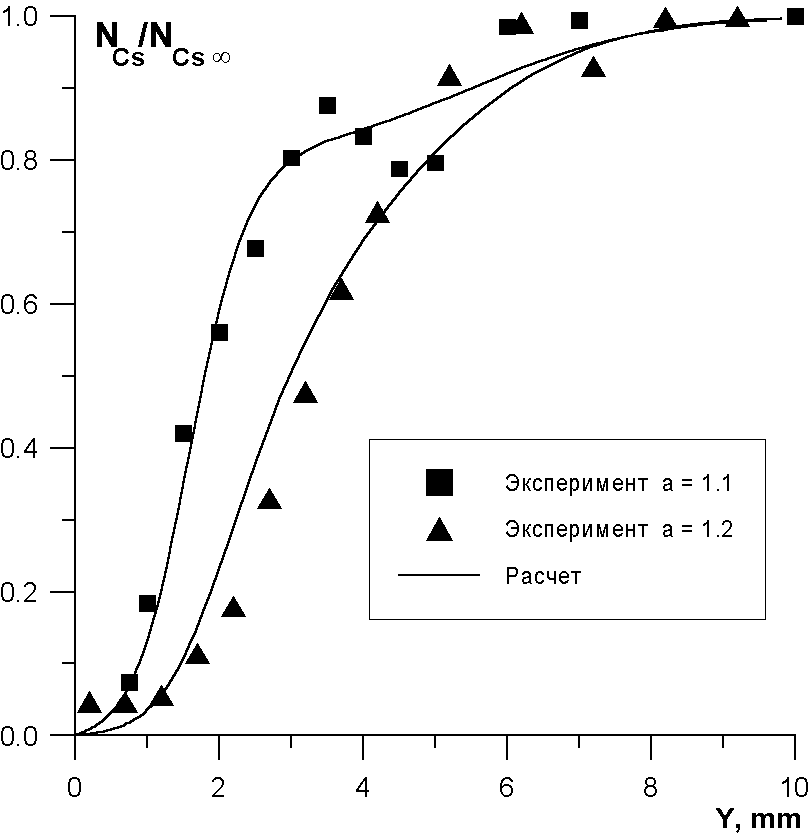
Измеренные и расчетные профили концентраций свободных атомов цезия в пограничном слое для 0.9<= a<= 1.2 и x =30мм для неохлаждаемой пластины представлены на Рис.3-4. Погрешность измерения концентрации не превышала 25%. Проведено исследование влияния наличия в продуктах сгорания гидрата цезия CsH на концентрацию свободных атомов цезия. Компьютерное моделирование физико-химических процессов в пограничном слое показало, что наибольшее влияние имеет место при a =0.9 (см. Рис.3), однако даже в этом случае оно незначительно. Поэтому в дальнейшем CsH был исключен из числа рассматриваемых компонент. Молекулярные массы Cs-содержащих компонент существенно превышают среднюю молекулярную массу смеси. Поэтому необходимо было исследовать влияние термодиффузии на процессы переноса этих компонент. Расчеты показали, что влияние этого эффекта является максимальным при a =0.9. Из Рис.3 видно, что эффект термодиффузии мало сказывается на профиле свободных атомов Cs в пограничном слое. |
.
 |
 |
| Рис.4 | Рис.5 |
На основе численного моделирования проведен анализ роли различных реакций с участием Cs-содержащих компонент на их распределение в пограничном слое при различных значениях параметра a . Этот анализ и сравнение результатов расчетов с экспериментом позволил определить достоверность значений констант химических реакций, приведенных в табл.1.
При a =0.9 доминирующими компонентами, содержащими цезий являются Cs и CsOH. Распределение этих компонент в пограничном слое определяется реакциями (2) и (3), из которых значение константы (2) известно из литературы. Поэтому результаты настоящих измерений и сравнение их с результатами численного моделирования позволило уточнить константу бимолекулярной реакции (3).
При a >= 1.1 доминирующими компонентами, содержащими цезий являются Cs и CsOH и CsO2. Распределение этих компонент в пограничном слое определяется реакциями (1), (3) и (4) из которых значение константы (1) известно из литературы, а значение константы (3) уточнено из анализа режима a =0.9. Поэтому анализ области a >= 1.1 позволил уточнить константу бимолекулярной реакции (4).
Расчеты показали, что реакции (5) и (6) слабо влияют на распределение Cs-содержащих компонент в пограничном слое в рассматриваемом диапазоне изменения коэффициента избытка окислителя a .
Сопоставление результатов численного расчета с результатами измерений показало, что предложенная модель химической кинетики с хорошей точностью описывает результаты измерений.
Литература
[ О Школе|Лекции|Секция 1|Секция 2|Секция 3|Секция 4|Секция 5|Cодержание |